
8月17日下午,北京科兴生物制品有限公司正式对外公布,由其生产的甲流感疫苗临床试验揭盲,初步结果显示“疫苗对人体安全有效”,据北京科兴负责媒体事务的刘沛诚透露:“以现在的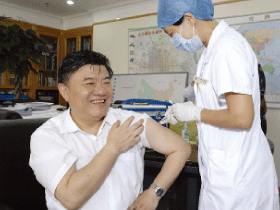 进度来看,比最初我们预计的时间整整提前了21天”,而这也被认为是 “全球首个完成初步评价的甲流疫苗临床试验”。
进度来看,比最初我们预计的时间整整提前了21天”,而这也被认为是 “全球首个完成初步评价的甲流疫苗临床试验”。
从7月22日开始临床试验算起,这次备受瞩目的临床试验已经过去26天。实际上,从7月10日 《甲型H1N1流感疫苗临床试验指导方案》正式出台之后,如何选择临床试验区域,如何招募并选定试验者,如何评价试验结果等重要细节,卫生部、国家食品药品监督管理局(SFDA)、中国疾病预防控制中心(CDC)、北京疾控中心和疫苗生产企业已经开始紧锣密鼓地开展起来。
怀柔试点
拿到甲流感毒株以后,对于企业而言,即意味着正式启动甲流感疫苗的研发与生产程序。因为是特殊时期,甲流感疫苗的生产审批肯定要走特殊审批程序,从时间上来看,启动甲流感疫苗临床试验也迫在眉睫。与药品的临床期试验不同的是,疫苗试验的程序、安全性要求都很高。
为此,卫生部、SFDA和中国CDC专门制定了一份 《甲型H1NI流感疫苗临床试验指导方案》,明确地界定了试验的设计方案、样本量、程序和计量以及研究终点的要求,“其严格与严谨程度超过以往。”中国CDC免疫规划中心的一位研究人员说。
试验区域放在怀柔并没有太大争议。尽管此前有很多北京市民都在民调中表示 “希望试点放在自己的居住区”,但选定区域不仅仅取决于个体的志愿意愿,还取决于区域政府的支持以及原有的临床试验基础。
综合这两个方面的关键性因素,怀柔区曾经作为人禽流感疫苗临床试验基地的优势凸显,因此在政府、研究机构与企业之间很快就达成了一致:怀柔再次作为甲流感疫苗临床试验基地。
由于怀柔区具有禽流感疫苗临床试验的经验,招募志愿者也是轻车熟路。#p#副标题#e#
7月初,怀柔区某事业单位工作人员王军就获悉了区疾控中心在招募甲流感疫苗临床试验志愿者的信息,随后王军就找到相关机构,主动报名参与临床试验,但他承认,“这次是偷偷报名的,上次向家人和女友公开提出要参加人用禽流感疫苗的临床试验,明确遭到了父母和女友的一致反对,他们担心疫苗试验会有副反应。”
王军是这次临床试验1614名志愿者中的一员,据了解,这批试验者中,大部分都是自己主动报名的,其中也有一部分是政府“做工作”才参与进来的,“最大的担心就是对这种新病毒心里没谱。”
另据了解,此次试验人员分老年组、成人组、少年组和儿童组,受试者总人数为1614例,其中60岁以上老年组101例,18-60岁成人组706例,12-17岁少年组404例,3-11岁儿童组403例。
接种程序为老年组接种1针;成人组、少年组和儿童组需要接种2针。试验疫苗共分3种类型:加佐剂灭活疫苗、加佐剂裂解疫苗、无佐剂裂解疫苗。第一针临床接种试验自7月22日清晨6点开始,至7月25日分批完成。
王军清楚地记得,报完名后,他很快就被告知已经正式作为“成人组志愿者”参与这次甲流感疫苗的临床试验,在接种疫苗之前,他还被告知要先签署知情同意书。“我曾经做过一次小手术,签过医院的知情同意书,无非就是告诉我这次参与试验可能要遇到的风险,我压根儿就没想那么多。倒是有听说,有人在看完知情同意书后,决定退出。”
签下知情同意书后,王军被安排进行了身体检测(包括问诊、体检、尿检),随后就接受了接种前的采血检测。22日下午,采完血的王军接种了第一针疫苗,在观察室呆了半个小时,没有出现任何反应,接种医生并没有告诉他接种的是哪一种疫苗,只是叮嘱他回家后“密切观察身体反应,如测体温并记录下来,有情况及时联系”,同时还要求他21天后还要来接种第二针。
这位医生还向王军透露说,所有志愿者都不知道自己接种的是三类疫苗中的哪一种,其中还有101人作为对照组,其实接种的只是一种叫做“PBS缓冲液”的安慰剂。
在接种完第一针后的前三天,王军接到了医生的电话询问,主要是问他的身体情况。也就在同一时间,中国CDC正式通报,“全部受试者已完成接种后3天的安全性观察,无严重不良反应事件报告。”
北京科兴方面透露,全部受试者的总体不良反应发生率11.8%,与季节性流感疫苗相似。不良反应以轻度、一过性的反应为主,主要症状为注射部位疼痛。“初步结果显示疫苗安全可靠”。
21天后的8月12日,除了只需接种一针的老年组,王军和其他1512名受试者接种了第二针,还需要再接受两次采血,用以检测疫苗安全性和志愿者身体状况。
两次接种,王军本人并没有出现任何不良反应。#p#副标题#e#
部长首试
8月11日和12日,全世界的主要媒体和门户网站都报道 “中国卫生部部长陈竺接种第二针甲流感疫苗”的消息,同时转载了陈竺接种疫苗的现场图片,由此也引发了各种热议。
据情人士透露,其实早在7月21日中午,陈竺就作为“国产甲流感疫苗临床试验的第一个接种者”。中国CDC的一位专家认为,中国是全世界第一个开展甲流感疫苗临床试验的国家,陈竺因此有可能是全世界第一个接种甲流感疫苗的人。从7月22日起,中国开始了大规模的甲流感疫苗临床试验。出于对志愿者的尊重,相关机构对志愿者的个人情况也处于严格保密状态,由此,陈竺也是少有几个被公开“试验人”身份的人。
一直到8月11日,陈竺作为甲流感疫苗临床试验者之一,一直无人知晓,事后也无人对此作出解释,由此也引发了各界的猜想。“其实也没什么,参与这次临床试验肯定是陈部长本人主动提出来的,之所以一开始没有通报媒体,可能还是对这种新型病毒疫苗的安全性和有效性存有担忧。”
这位知情人士还透露,在接种第一针的时候,陈竺就对新疫苗表现出了完全的信心,接种过程中也是“表情轻松,谈笑风生”,倒是周围的人捏了一把汗。3天安全性观察,也无异常,“这让所有的人都松了一口气,进而认为有必要在接种第二针的时候,将这个信息公开。主要的目的是要提升国人对国产甲流感疫苗的信心。”
据负责为陈竺接种的工作人员介绍,每次为陈竺注射疫苗(2次)或抽血化验(3次)的时候,他都是满脸笑容,表现得信心十足。陈竺曾私下告诉工作人员,之所以率先接种国产的甲流疫苗,就是要表明自己的信心和决心,他相信中国生产的疫苗质量不比跨国公司的差。
作为中国卫生部长的陈竺,以志愿者的身份参与新疫苗的临床试验的消息公开以后,也引起了很多在华外媒的关注,一些外媒记者纷纷透过各种打探渠道,询问陈竺部长接种甲流感疫苗过程中的一些细节,也有外媒直接撰文对陈竺的这一行为寄予高度评价,认为“这样的举动恰恰是反映了一种对自主研制的疫苗的一种自信,在今后的疫苗推广过程中将非常具有典范意义”。#p#副标题#e#
安全性争议
8月17日下午,北京科兴的甲流感疫苗揭盲会上,相关专家透露本次临床试验共有1614名3岁以上的受试者完成疫苗接种及血样采集,中国药品生物制品检定所完成了全部血清的血凝抑制抗体(HI抗体)检测。
分析结果显示,临床试验用疫苗在接种一针后可产生良好的免疫反应,保护性抗体阳性率、抗体阳转率和几何平均滴度(GMT)增长倍数三项指标均达到疫苗评价标准,表明接种疫苗可以对人体产生保护。
北京科兴生物制品有限公司总经理尹卫东也向媒体透露:“疫苗接种后的14天和21天的血清结果表明,疫苗产生了良好的有效性反应和良好的抗体反应,也就是达到了预期的效果,因此说这个疫苗的临床研究在有效性上取得了圆满的效果。”
尹卫东还说:“将迅速地把已经有的安全性数据进行整理,完成一份医学报告,然后上报国家食品药品监督管理局,申请疫苗的批准文号。另外还会把系统的科学研究整理出科学论文,给国际上提供翔实的科学数据,为全球甲型H1N1流感防控提供很好的信息,当然也在紧锣密鼓地进行甲型H1N1流感疫苗的生产,希望尽快有更多的疫苗提供给甲型H1N1流感防控。”
据了解,这次完成的甲型H1N1流感疫苗的临床试验,可以确定疫苗的免疫程序和剂量,为国家制定甲型H1N1流感疫苗的使用策略提供科学依据。对于疫苗生产而言,也将由此启动“特别审批”程序。
不过,这种“特别审批”也引来了专家的不同声音,甚至担忧。
军事医学科学院微生物流行病研究所研究员祝庆余教授此前表示,应该关注疫苗的安全性和有效性,虽然现在已生产出了临床前疫苗,但距离它真正用到社会大众身上,还得再等一段时间。
对于安全性的争议,甚至有人搬出了发生在1976年的美国的疫苗事件,对此发出警告。1976年,美国在发现人感染猪流感病例后先后对数千人接种疫苗,但其中数百人因此出现自身免疫性疾病“吉兰-巴雷综合征”——病人大多全身瘫痪,严重者呼吸肌麻痹,不能吞咽,死亡率高达25%以上。
7月25日举行的全国食品药品监督管理工作座谈会上,对于甲型H1N1流感疫苗的审评审批,卫生部副部长、国家食品药品监督管理局局长邵明立公开强调,安全有效是甲型H1N1流感疫苗生产、储备和使用的前提,时间再紧,疫苗的审评审批也要坚持科学依法、程序不减、标准不降的要求。绝不能因为赶时间、保数量、交任务而放松安全性要求。
【欢迎转载 请注明来源】